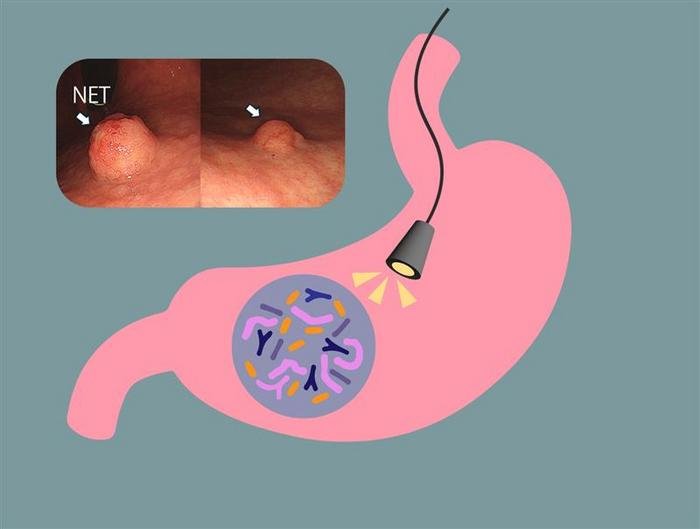
Forscher der Osaka Metropolitan University haben herausgefunden, wie sich das Bakteriengleichgewicht im Magen auf das Wachstum neuroendokriner Tumoren (NETs) auswirkt. Durch die Identifizierung der beteiligten Bakterien und der biochemischen Reaktionen, die das Tumorwachstum verursachen, hoffen die Forscher, ein neues Diagnoseverfahren zu entwickeln, um Patienten mit hohem Krebsrisiko zu identifizieren.
Autoimmungastritis (AIG) ist eine chronische Erkrankung, bei der das körpereigene Immunsystem fälschlicherweise die Magenschleimhaut angreift. Diese anhaltende Immunreaktion schädigt den Magen allmählich und beeinträchtigt seine Funktion und seine Fähigkeit, sich vor schädlichen Einflüssen zu schützen. Mit der Zeit können diese Veränderungen das Risiko für die Entwicklung von NETs erhöhen, einer Tumorart, die sich aus hormonproduzierenden Zellen im Magen entwickelt.
Der Magen beherbergt die Magenmikrobiota, eine vielfältige Gemeinschaft von Mikroorganismen, die für die Erhaltung der Gesundheit wichtig sind. Die Forschungsgruppe um Dr. Koji Otani von der Osaka Metropolitan University Graduate School of Medicine analysierte Veränderungen der Magenmikrobiota und der aus Gewebe gewonnenen Metaboliten anhand von DNA aus Biopsieproben, um zu verstehen, wie diese Mikroorganismen bei AIG-Patienten beeinflusst werden. Das Verständnis dieses Prozesses könnte dazu beitragen, die Entstehung von Tumoren im Magen zu verstehen.
Bei Patienten wird die „?-Diversität“ häufig zur Beurteilung der Darmgesundheit herangezogen, da sie die Anzahl der verschiedenen mikrobiellen Arten in einer bestimmten Probe widerspiegelt. Eine hohe ?-Diversität ist normalerweise ein Zeichen für einen gesunden, ausgeglichenen Darm; bei AIG-Patienten wurde jedoch eine verringerte ?-Diversität festgestellt.
Interessanterweise wurden unterschiedliche Bakteriengemeinschaften beobachtet, je nachdem, ob der Patient NET entwickelt hatte oder nicht. Dies wurde durch eine Heatmap-Analyse der relativen Häufigkeit der Magenmikrobiota unterstützt, die unterschiedliche Zusammensetzungsmuster in der Gruppe mit NET-Entwicklung aufzeigte.
Insbesondere die NET-positive Gruppe wies erhöhte Werte von Haemophilus parainfluenzae und Fusobacterium -Arten auf, insbesondere F. periodonticum und F. nucleatum . Während diese Bakterien typischerweise in gesunden Mägen vorkommen, sind erhöhte Werte oft für entzündliche Erkrankungen verantwortlich.
Darüber hinaus stellten sie einen Rückgang der Milchsäurebakterien und des Streptococcus salivarius fest , die an der Erhaltung der Gesundheit beteiligt sind und üblicherweise schädliche Bakterien hemmen.
Die Gruppe untersuchte die ablaufenden biochemischen Reaktionen mithilfe metabolomischer Analysen. Sie fanden heraus, dass die Zellen von AIG-Patienten im Vergleich zu normalem Gewebe ihre Art der Energieerzeugung und -nutzung veränderten (ein Prozess, der als metabolische Neuprogrammierung bezeichnet wird).
Diese metabolische Umprogrammierung war durch eine verringerte Aktivität in den Glykolyse- und TCA-Zykluswegen gekennzeichnet, die üblicherweise zur Energiegewinnung genutzt werden. Stattdessen verlagerte sich der Stoffwechsel auf alternative Wege, um den Energiebedarf zu decken. Diese Stoffwechselverlagerung kann die Zellfunktion sowie Entzündungen und Gewebeumbauprozesse beeinträchtigen.
Die Forscher kamen zu dem Schluss, dass bestimmte Gewebestoffwechselmuster mit AIG und bestimmte Signaturen der Magenmikrobiota mit der Entwicklung von Magen-NETs assoziiert sind. „Die Studie legt nahe, dass bei AIG-Patienten Veränderungen im Stoffwechsel des Wirtes vor Veränderungen der Magenmikrobiota auftreten. Dadurch entsteht möglicherweise ein Mikromilieu, das das Wachstum von Bakterien begünstigt, die mit der Bildung von Magen-NETs in Verbindung stehen“, erklärte Dr. Otani. „Unsere Ergebnisse sollen das Verständnis des Verlaufs vom Beginn der AIG bis zur Entwicklung von Magen-NETs verbessern und die Entwicklung neuer diagnostischer Marker für Früherkennung und Prävention unterstützen.“

Credits
Osaka Metropolitan University
Die Studie wurde im Journal of Gastroenterology veröffentlicht.