Mithilfe lichtinduzierbarer Genexpression konnten Wissenschaftler zeigen, dass die Bildung der Körperachsen in menschlichen Embryomodellen ein Zusammenspiel zwischen chemischen Signalen und mechanischen Kräften erfordert.
Bereits zwei Wochen nach der Befruchtung zeigen sich erste Anzeichen für die Ausbildung der drei Körperachsen (Kopf/Schwanz, Bauch/Rücken und rechts/links). In diesem Stadium, der sogenannten Gastrulation, faltet sich eine flache, strukturlose Zellschicht zu einem lebenden Bauplan des Körpers – eine flüchtige Transformation in Achsen und Schichten, die die Entwicklung jedes einzelnen Gewebes bestimmen. Dieser entscheidende Moment blieb jedoch lange Zeit der wissenschaftlichen Forschung entzogen, da er zu früh und zu tief im Mutterleib stattfindet, um direkt untersucht zu werden.
Eine neue Studie zeigt nun, dass dieser entscheidende Schritt der menschlichen Entwicklung durch ein präzises Zusammenspiel chemischer Signale und physikalischer Kräfte gesteuert wird. Die in Cell Stem Cell veröffentlichte Arbeit stellt ein lichtbasiertes Werkzeug zur Erzeugung synthetischer Embryonen vor, mit dem Forscher wichtige Entwicklungsproteine ??aktivieren können, die bekanntermaßen die Gastrulation einleiten. Als das Team eines dieser Proteine, BMP4, mithilfe von Licht aktivierte, stellten sie fest, dass chemische Signale allein nicht ausreichten – die Transformation setzte erst ein, wenn die Zellen auch den richtigen mechanischen Bedingungen ausgesetzt waren. Die Ergebnisse belegen eine grundlegende Wechselwirkung zwischen Gewebemechanik und molekularer Signalgebung und bieten ein realistischeres Modell der frühen menschlichen Entwicklung sowie eine potenzielle Grundlage für zukünftige regenerative Therapien und Fruchtbarkeitsbehandlungen.
Die Gastrulation beginnt mit der Symmetriebrechung. Eine einheitliche Schicht embryonaler Zellen ordnet sich dreidimensionalen Kopf-Schwanz-Achsen zu – dem räumlichen Bauplan, der die spätere Position von Kopf, Wirbelsäule und Gliedmaßen bestimmt. Brivanlou und seine Kollegen erforschen seit Jahrzehnten mithilfe von Tiermodellen und Laborstudien mit humanen embryonalen Stammzellen dieses entscheidende Entwicklungsstadium. „Die Gastrulation findet kurz nach der Einnistung in der Gebärmutter statt und kann daher in vitro nur mit Hilfe humaner pluripotenter Stammzellen untersucht werden “, erklärt Riccardo De Santis, Direktor des Human Pluripotent Stem Cell Resource Center an der Rockefeller University und gemeinsam mit dem theoretischen Physiker Laurent Jutras-Dubé Erstautor dieser Studie. „Unser Ziel war es, einen Einblick in einen Entwicklungsschritt zu gewinnen, der in vivo sonst nicht untersucht werden kann .“
Frühere Arbeiten zeigten, dass biochemische Signalmoleküle wie BMP4 das Verhalten von Zellen und Geweben beeinflussen und so die Embryonalentwicklung regulieren. Studien an Frosch- und Hühnerembryonen legten jedoch nahe, dass dies nur ein Teilaspekt ist. Mechanische Spannungen, die Gewebegeometrie und verschiedene physikalische Kräfte scheinen ebenfalls eine Rolle bei der Entwicklung tierischer Embryonen zu spielen. „Jetzt liegen endlich viele Daten vor, und es ist klar, dass die Bedeutung mechanischer Signale bisher unterschätzt wurde“, sagt De Santis.
De Santis entwickelte ein optogenetisches Werkzeug, mit dem sein Team das Zusammenspiel biochemischer Signale und mechanischer Kräfte im Kontext der menschlichen Entwicklung untersuchen kann. Durch die gezielte Veränderung menschlicher embryonaler Stammzellen, sodass diese auf Licht reagieren, ermöglichte sein System den Forschern die Aktivierung von Entwicklungsgene mit außergewöhnlicher Präzision. Bei Bestrahlung mit Licht einer bestimmten Wellenlänge legten die Zellen einen genetischen Schalter um, der BMP4 dauerhaft aktivierte. Dieses System erlaubte es den Wissenschaftlern zudem, genau zu bestimmen, wann und wo das Signal im Zellverband aktiviert wird. So konnten sie erstmals untersuchen, wie Gewebegeometrie und mechanische Belastung an beliebigen Stellen im Embryo die Entwicklung beeinflussen.
Der Aufstieg mechanischer Kräfte
Als das Team dieses lichtbasierte System nutzte, um die BMP4-Signalübertragung in menschlichen Stammzellen zu aktivieren, wurde die Rolle mechanischer Kräfte schnell deutlich. In Kulturen, in denen BMP4 in einer unbeschränkten, spannungsarmen Umgebung aktiviert wurde, kam es nie zu einer vollständigen Gastrulation. BMP4 allein reichte zwar aus, um extraembryonale Zelltypen wie die Amnionzellen hervorzubringen, doch die Probe konnte weder Mesoderm noch Endoderm, die Keimblätter für die Organbildung, generieren. Dies zeigte, dass Morphogene allein für die Gastrulation nicht ausreichen.
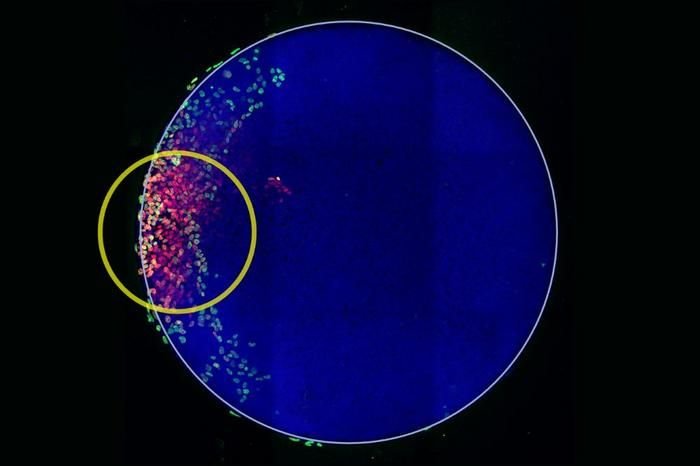
Credits:
Brivanlou-Labor/Rockefeller-Universität
Als das Team jedoch seine „Fernsteuerung“ auf die Ränder eingeschlossener Zellkolonien und auf in spannungsinduzierende Hydrogele eingebettete Zellen richtete, begannen sich die für die Gastrulation fehlenden Schichten zu bilden. Weitere Experimente zeigten, wie mechanische Spannung über YAP1 die nachgeschalteten biochemischen Signalwege, vermittelt durch WNT und Nodal, feinabstimmt, welche den Zellen signalisieren, zu welchen Gewebetypen sie sich entwickeln sollen. Eine frühere Studie unter der Leitung von Senior Research Associate Francesco Piccolo in Zusammenarbeit mit dem verstorbenen Jim Hudspeth, Leiter des Labors für sensorische Neurowissenschaften an der Rockefeller University, demonstrierte, dass die nukleären Konzentrationen des Mechanosensorproteins YAP1 eine entscheidende Rolle bei der Regulierung der Selbstorganisation in Mikrostrukturen spielen (Piccolo et al., 2022). Die vorliegende Studie enthüllte, dass nukleäres YAP1 als molekulare Bremse der Gastrulation wirkt und verhindert, dass diese Transformationen zu früh erfolgen. Die Ergebnisse legen nahe, dass die Gastrulation nur dann beginnen kann, wenn molekulare Signale und mechanische Spannung übereinstimmen – die Zellen müssen demnach sowohl chemisch vorbereitet als auch physikalisch aktiviert sein.

