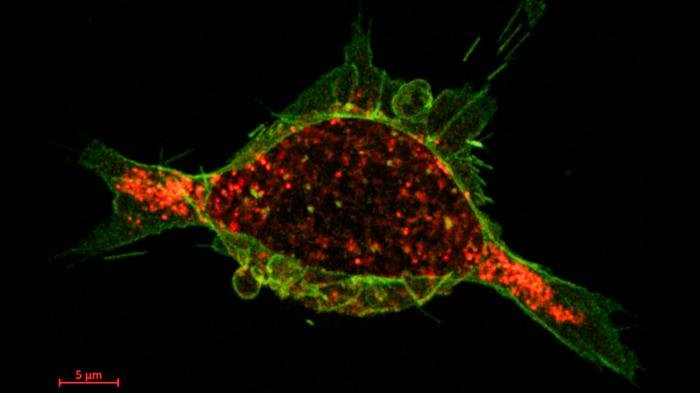
Antikörpermedikamente zur Krebsbekämpfung sind so konzipiert, dass sie in Tumorzellen eindringen und dort eine tödliche Substanz freisetzen. Doch allzu oft erreichen sie dieses Ziel nicht. Eine neue Studie zeigt, wie diese Strategie – ähnlich einem Trojanischen Pferd – durch die Ausnutzung von Kalziumunterschieden innerhalb und außerhalb der Zellen effektiver funktioniert.
Ein Forschungsteam unter der Leitung von Sophia Hober, Professorin am KTH Royal Institute of Technology, hat die Entwicklung eines Kalzium-aktivierten Wirkstoffabgabesystems vorgestellt. Dieses System soll eine präzisere Behandlung mit niedrigeren Dosen und weniger Schäden an gesundem Gewebe ermöglichen. In Zusammenarbeit mit der Stanford University und der Universität Umeå veröffentlichten die Forscher ihre Ergebnisse in PNAS , der Fachzeitschrift der National Academy of Sciences.
Das Konzept zielt auf eine häufige Herausforderung bei zielgerichteten Medikamenten ab, die dazu neigen, sich zu stark an Rezeptoren von Tumoren anzulagern. Positiv ist, dass diese starke Bindung die Wachstumssignale der Rezeptoren blockiert. Antikörper-Wirkstoff-Konjugate (ADCs) sollen jedoch auch Zellen angreifen und abtöten. Allzu oft bleibt das Protein jedoch hängen, ohne tiefer in die Zelle einzudringen und ihr eigentliches Ziel zu erreichen: das saure Kompartiment, das Lysosom. Dort, in der sogenannten „Abtötungszone“, kann das Zielprotein abgebaut werden, wodurch ein Toxin freigesetzt wird, das zum Zelltod führt.
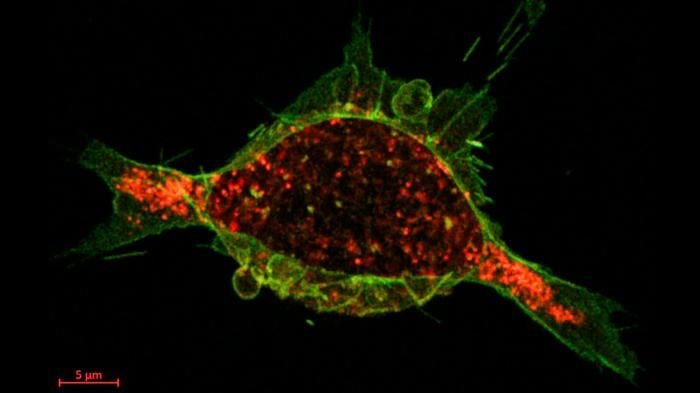
Credits
KTH Royal Institute of Technology
Um dieses Problem zu vermeiden, entwickelten die Forscher einen kalziumempfindlichen Schalter, der stark an den Krebszellrezeptor auf der Außenseite der Zelle bindet, wo relativ hohe Kalziumkonzentrationen im Blut und in der extrazellulären Flüssigkeit vorkommen.
Sobald das mit dem Wirkstoff beladene Protein (oder die calciumregulierte Affinität, CaRA) ??und der epidermale Wachstumsfaktorrezeptor (EGFR) miteinander verbunden sind, werden sie in die Zelle in Kompartimente mit allmählich sinkenden Calciumkonzentrationen transportiert. Da ihre Bindung calciumabhängig ist, trennen sich die Wege von Rezeptor und CaRA schließlich: Der Rezeptor kann zur Membran zurückkehren, während CaRA seine Fracht weiterhin zum Lysosom transportiert.
„Der Kalziumschalter ist in das Medikamentendesign integriert“, sagt Hober. „Er misst den Kalziumspiegel und ändert seine Bindungsstärke automatisch.“