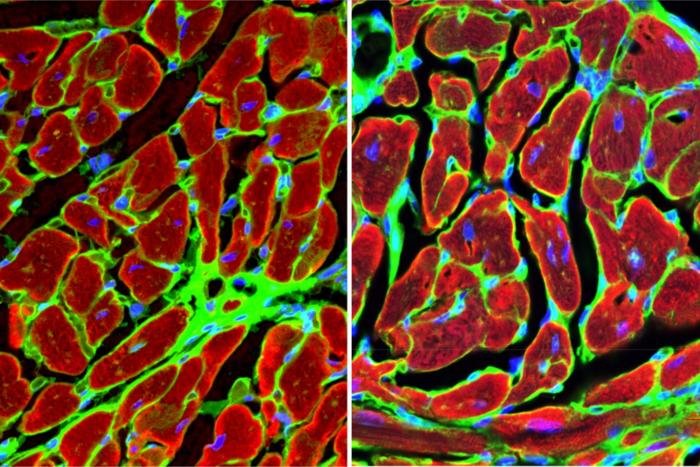
Wissenschaftler der UCLA haben das Protein GPNMB als entscheidenden Regulator im Heilungsprozess des Herzens nach einem Herzinfarkt identifiziert.
Anhand von Tiermodellen konnten sie nachweisen, dass aus dem Knochenmark stammende Immunzellen, sogenannte Makrophagen, GPNMB absondern, das an den Rezeptor GPR39 bindet und so die Herzreparatur fördert. Diese Erkenntnisse bieten ein neues Verständnis davon, wie das Herz sich selbst heilt, und könnten zu neuen Behandlungen führen, die darauf abzielen, die Herzfunktion zu verbessern und das Fortschreiten einer Herzinsuffizienz zu verhindern.

Credits:
Arjun Deb Lab/UCLA
Frühere klinische Studien haben gezeigt, dass GPNMB (Glycoprotein Non-Metastatic Melanoma Protein B) stark mit kardiovaskulären Folgen bei Personen mit Herzinsuffizienz in Zusammenhang steht. Unklar war jedoch, ob das Fehlen des Proteins direkt für die Entwicklung einer Herzinsuffizienz nach einem Herzinfarkt verantwortlich ist. Diese wichtige Unterscheidung – ob GPNMB nur ein assoziierter Biomarker ist oder eine kausale Rolle spielt – bestimmt, ob das Protein als therapeutisches Ziel für zukünftige Studien in Betracht gezogen werden kann.
Anhand von Mausmodellen stellten die Forscher zunächst fest, dass GPNMB nicht vom Herzen selbst exprimiert wird, sondern von Entzündungszellen aus dem Knochenmark produziert wird. Nach einem Herzinfarkt wandern diese Makrophagen zur verletzten Stelle im Herzen, wo sie GPNMB exprimieren.
Das Team führte Gen-Knockouts durch – die Inaktivierung des GPNMB-Gens – [AS1] und Knochenmarktransplantationen und beobachtete, dass Mäuse ohne das GPNMB-Gen nach einem Herzinfarkt dramatisch schlechtere Ergebnisse zeigten, darunter eine höhere Inzidenz von Herzrupturen, einer tödlichen Komplikation, die auch bei menschlichen Herzinsuffizienzpatienten auftritt. Umgekehrt zeigten Mäuse mit normaler GPNMB-Expression, denen eine zusätzliche Dosis des zirkulierenden GPNMB-Proteins verabreicht wurde, eine verbesserte Herzfunktion und weniger Narbenbildung. Vier Wochen nach einem simulierten Herzinfarkt wiesen 67 % der Tiere ohne das GPNMB-Gen eine schwere Fibrose oder Narbenbildung auf, verglichen mit nur 8 % der Tiere in der Kontrollgruppe.
Die Forscher identifizierten GPNMB nicht nur als Signalmolekül mit Wirkungen auf verschiedene Zelltypen, sondern entdeckten auch, dass es an GPR39 bindet, das zuvor als Orphan-Rezeptor galt, also als Rezeptor, dessen Bindungspartner unbekannt ist. Diese Interaktion löst eine Signalkaskade aus, die die Geweberegeneration fördert und die Narbenbildung begrenzt.
Original Paper:
https://www.nature.com/articles/s44161-024-00555-4