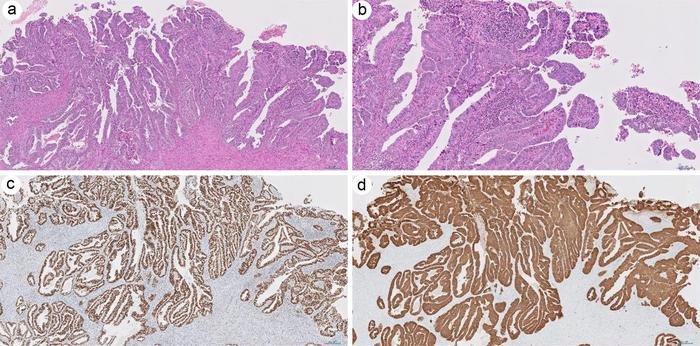
Endometriumkarzinom ist eine der häufigsten gynäkologischen Krebserkrankungen. Zu den HGEC gehören aggressive Varianten wie endometrioide Karzinome Grad 3, seröse, klarzellige, undifferenzierte/dedifferenzierte Karzinome, Karzinosarkome und mesonephrische Adenokarzinome. Diese Tumoren zeichnen sich durch eine schlechte Prognose und Resistenz gegenüber konventionellen Therapien aus. Die Einschränkungen der traditionellen histopathologischen Diagnose unterstreichen die Notwendigkeit molekularer Verbesserungen zur Steuerung der klinischen Behandlung.
Histopathologische Subtypen von HGEC
- FIGO Grad 3 Endometrioides Karzinom (HG-EEC): Charakterisiert durch >50 % solide Architektur, häufig aufgrund einer Endometriumhyperplasie. Molekulare Veränderungen umfassen den Verlust von ARID1A, PTEN oder Mismatch-Reparatur-Proteinen (MMR), mit aberrantem p53 in etwa 20 % der Fälle.
- Seröses Karzinom: Präsentiert sich typischerweise im atrophischen Endometrium mit komplexer papillärer Architektur, hochgradigen Kernen und häufigen TP53-Mutationen. Es fällt in die Gruppe der TCGA-Kopienzahl-hohen (CNH) und hat eine schlechte Prognose.
- Undifferenziertes und dedifferenziertes Karzinom (UC/DDC): Hochaggressive Tumoren mit Verlust der epithelialen Kohäsion und häufigen SWI/SNF-Komplexmutationen. Häufig zeigen sie MMR-Mangel oder POLE-Mutationen.
- Uteruskarzinosarkom (UCS): Zweiphasiger Tumor mit karzinomatösen und sarkomatösen Elementen. Molekular ähnlich dem serösen Karzinom, mit häufigen TP53- und PPP2R1A-Mutationen.
- Klarzelliges Karzinom (ECCC): Zeigt tubulozystische, papilläre oder solide Muster mit klaren oder oxyphilen Zellen. Zeigt häufig HNF-1?-Positivität und fällt sowohl in die CNH- als auch in die NSMP-Gruppe (kein spezifisches molekulares Profil).
- Mesonephrosen-ähnliches Adenokarzinom (MLA): Ein seltener, aggressiver Subtyp mit Müller- und Mesonephrosen-Merkmalen, oft KRAS-mutiert und hauptsächlich als Kopienzahl niedrig (CNL)/NSMP klassifiziert.
Molekulare Klassifizierung der TCGA
Die TCGA-Initiative hat Endometriumkarzinome in vier molekulare Untergruppen neu klassifiziert:
- POLE-ultramutiert: Hohe Mutationslast, ausgezeichnete Prognose, starke Immuninfiltration.
- MMR-defizient (MSI): Hypermutiert, mittlere Prognose, spricht auf Immuntherapie an.
- Hohe Kopienzahl (p53-abnormal): TP53-Mutationen, schlechte Prognose, umfasst seröse und viele Karzinosarkome.
- Niedrige Kopienzahl (NSMP): Mittleres Risiko, heterogen, umfasst viele endometrioide und klarzellige Karzinome.
Diese molekulare Schichtung liefert reproduzierbare, prognostisch bedeutsame Kategorien, die die Histologie ergänzen und eine gezielte Therapie ermöglichen.
Integration in die klinische Praxis
: NGS bleibt der Goldstandard für die molekulare Subtypisierung, immunhistochemische Surrogatmarker (z. B. p53, MMR-Proteine) ermöglichen eine einfache Klassifizierung. POLE- und MSI-Tumoren können von einer Immuntherapie profitieren, während CNH-Tumoren auf PARP- oder HER2-gerichtete Wirkstoffe ansprechen können. Die NSMP-Gruppe erfordert eine weitere Substratifizierung anhand zusätzlicher Marker wie L1CAM oder CTNNB1.
Herausforderungen und zukünftige Entwicklungen:
Zu den Hindernissen bei der Umsetzung zählen die Kosten, der Zugang zur Sequenzierung und die Notwendigkeit prospektiver Studien zur Validierung molekular gesteuerter Therapien. Weitere Forschung ist erforderlich, um die Klassifizierung innerhalb der NSMP-Gruppe zu verfeinern und die diagnostische Konsistenz zwischen den Institutionen zu verbessern.
Schlussfolgerung:
Die Integration der histopathologischen Untersuchung in die TCGA-basierte molekulare Profilierung stellt einen bedeutenden Fortschritt im Management von HGEC dar. Dieser Ansatz ermöglicht eine präzise Risikostratifizierung, unterstützt therapeutische Entscheidungen und unterstreicht die Bedeutung der Präzisionsonkologie für die Verbesserung der Patientenergebnisse. Kontinuierliche Bemühungen, molekulare Erkenntnisse mit der klinischen Praxis zu verknüpfen, sind unerlässlich, um der Heterogenität und Aggressivität von HGEC gerecht zu werden.
Volltext
https://www.xiahepublishing.com/2771-165X/JCTP-2025-00021
Die Studie wurde kürzlich im Journal of Clinical and Translational Pathology veröffentlicht .

Credits:
Zaibo Li, Himani Kuma