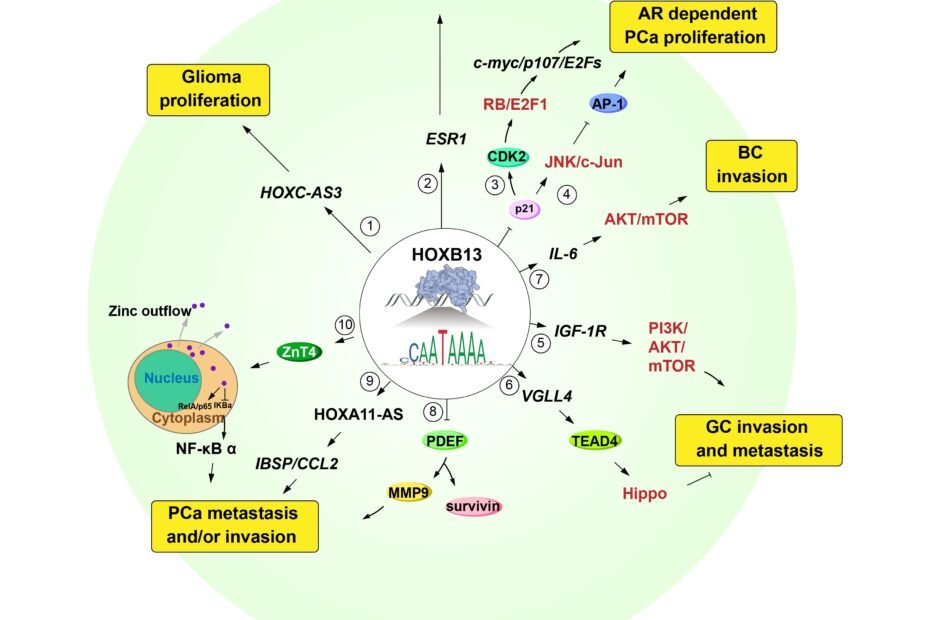
HOXB13, ein Homöobox-Transkriptionsfaktor der Klasse B, spielt eine zentrale Rolle in der Prostatakrebsforschung, sowohl in der Früherkennung als auch in der Therapie. Eine Studie, veröffentlicht am 7. August 2025 in Frontiers of Medicine (DOI: 10.1007/s11684-024-1119-x), zeigt, dass HOXB13-Transkripte im Urin als nicht-invasive Biomarker die Früherkennung von Prostatakrebs verbessern können, während Gewebespiegel helfen, Patienten für gezielte Therapien wie AR- oder BET-Bromodomain-Hemmung zu stratifizieren.

Die Untersuchung hebt die dualistische Natur von HOXB13 hervor, das je nach Kontext als Onkogen oder Tumorsuppressor wirkt. In der Prostata bildet HOXB13 mit MEIS1 Heterodimere, die die Androgenrezeptor (AR)-Signalisierung unterdrücken und den Tumorsuppressor Decorin fördern. Keimbahnmutationen wie G84E, die bei 3,5 Prozent der Finnen vorkommt, stören diese Bindung, fördern die Zusammenarbeit mit AR-V7-Spleißvarianten und treiben die Tumorentwicklung an. Diese Mutation ist in Ostasien nahezu absent, was geografische Unterschiede in der klinischen Strategie unterstreicht. Screening-Leitlinien empfehlen für G84E-Träger PSA-Tests ab 40 Jahren, während Multiplex-Panels mit HOXB13, BRCA2 und ATM die Risikovorhersage verbessern.
Therapeutisch zeigen HDAC4-Inhibitoren wie Natriumbutyrat die Fähigkeit, HOXB13 in AR-negativen Prostatatumoren zu reaktivieren. Der BET-Antagonist JQ1 verdrängt BRD4 vom HOXB13-Promotor, und DNMT-Inhibitoren kehren CpG-Hypermethylierung um, etwa bei Darmkrebs. Retinsäure oder EZH2-Blockade reduziert H3K27me3, wodurch die tumorsuppressive Funktion von HOXB13 wiederhergestellt wird. Decorin und CHD1 unterbrechen die HOXB13-AR- oder HOXB13-MEIS1-Schnittstellen, was die Kastrationsresistenz begrenzt. Phase-II-Studien kombinieren BET- und PI3K-Inhibitoren, um die HOXB13-Sucht bei metastasiertem kastrationsresistentem Prostatakrebs zu nutzen.
Auf molekularer Ebene wird HOXB13 durch komplexe epigenetische Mechanismen reguliert. In Prostatakrebs fördert BRD4 die H3K27ac-Ablagerung am HOXB13-Promotor, was die Überexpression antreibt. In Endometriumkarzinomen und Gliomen führt EZH2-vermitteltes H3K27me3 oder YY1-rekrutiertes HDAC4 zur Stummschaltung. CpG-Methylierung und m6A-Editing der mRNA beeinflussen die Expression, während posttranslationale Modifikationen wie Acetylierung durch CREB oder Phosphorylierung durch mTOR die Funktion von HOXB13 zwischen tumorfördernd und -hemmend umschalten.
Zukünftig könnten Einzelzell-Multiomik und räumliche Transkriptomik die HOXB13-Netzwerke in der Tumormikroumgebung detailliert kartieren, um Präzisionskombinationen für personalisierte Therapien zu entwickeln. Die Immunhistochemie für HOXB13 verbessert bereits die Diagnostik, etwa zur Unterscheidung von Prostatakrebs und Urothelkarzinom, während das HOXB13/IL17B-Verhältnis bei Brustkrebs Therapieentscheidungen unterstützt. Diese Fortschritte versprechen eine verbesserte Früherkennung und Behandlung von Prostatakrebs und anderen Tumoren.
Original Paper:
HOXB13 in cancer development: molecular mechanisms and clinical implications